| Содержание |
Величина |
Наименование |
М - масса одного моля данного вещества. Вычисляется по таблице Менделеева, в которой массовое число численно равно молярной массе в граммах на моль. Для перевода единиц в систему СИ (кг/моль), необходимо это число уменьшить в 1000 раз.
 Молярная масса сложных молекул является суммой масс, составляющих их атомов. Молярная масса сложных молекул является суммой масс, составляющих их атомов.
Пример: молярная масса СО2 равна (по таблице Менделеева: углерод 12 + кислород 16·2 = 32) 44 г/моль = 0,044 кг/моль.
Формулы, где встречается молярная масса:
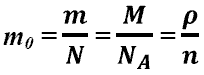 Масса молекулы. Масса молекулы.
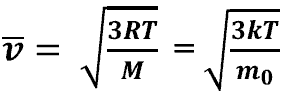 Средняя скорость молекул Средняя скорость молекул
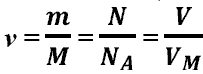 Количество вещества Количество вещества
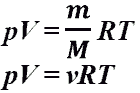 Уравнение Менделеева-Клайперона Уравнение Менделеева-Клайперона
 Изменение внутренней энергии идеального одноатомного газа. Изменение внутренней энергии идеального одноатомного газа.
|
М - молярная масса (см. в табл. Менделеева или в справочных таблицах) |
кг/моль |
| n - концентрация молекул |
1/м3 |
| ν - количество вещества |
моль |
| p - давление |
Па = Н/м2 |
| N - число молекул |
- |
| NA= 6,02 . 1023 - число Авогадро, число молекул в 1 моле |
1/моль |
| T - абсолютная температура газа (to + 273) |
К |
| Eк - средняя кинетическая энергия молекул газа |
Дж |
| k = 1,38 . 10-23 |
Дж/К |
| V - объем газа |
м3 |
| m0 - масса молекулы |
кг |
| m - масса газа |
кг |
| ρ - плотность газа |
кг/м3 |
| v - средняя скорость молекул газа |
м/с |
| R = 8,31 - универсальная газовая постоянная |
Дж/К моль |
| ΔU - изменение внутренней энергии |
Дж |
 Молярная масса сложных молекул является суммой масс, составляющих их атомов.
Молярная масса сложных молекул является суммой масс, составляющих их атомов.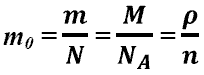 Масса молекулы.
Масса молекулы.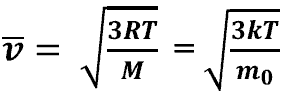 Средняя скорость молекул
Средняя скорость молекул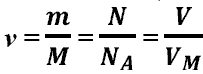 Количество вещества
Количество вещества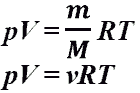 Уравнение Менделеева-Клайперона
Уравнение Менделеева-Клайперона Изменение внутренней энергии идеального одноатомного газа.
Изменение внутренней энергии идеального одноатомного газа.